丝素蛋白(SF)以其良好的生物相容性、优异的力学性能、可调节的生物降解性和较小的炎症反应等优势在组织工程领域得到了广泛的应用。心脏和肝脏等较厚组织的血管化是临床面临的一个巨大挑战。距离最近的毛细血管100-200微米的细胞和组织将受到缺氧和营养不良等不良条件的影响,容易造成细胞凋亡。因此,较厚的组织工程支架的生存能力取决于组织的血管化。
目前丝素蛋白支架的常用制备方法如冷冻干燥、静电纺丝等方法制备的丝素蛋白支架均可溶于水,需要有机溶剂进行后处理以获得具有水不溶性的稳定结构。但是,有机溶剂难以完全去除,而残留的有机溶剂不利于细胞的黏附、增殖以及组织的新生。本实验室开发了一种简单的制备方法,可以通过调节冷冻温度控制丝素蛋白分子的活性直接形成不溶于水的丝素蛋白多孔支架。将丝素蛋白溶液冷冻保存,以维持其浓缩状态,然后通过调节储存温度来控制丝素蛋白分子的活性。通过调节冷冻温度、冷冻时间这两个因素,直接得到无需任何预/后处理的丝素蛋白三维多孔支架。该支架成型过程条件温和,有利于生物活性分子的保存。
我们进一步通过批量加载制备了REDV多肽与丝素蛋白复合的多孔支架来增强厚组织的血管化,避免了有机溶剂和其他有毒副作用的化学品的使用。研究结果表明REDV/SF复合支架材料具有优异的诱导血管化性能,有潜力应用于复杂组织的修复。此外,其他活性分子也可以通过类似的途径与丝素支架结合,该方法可以广泛应用于组织工程的其他领域。
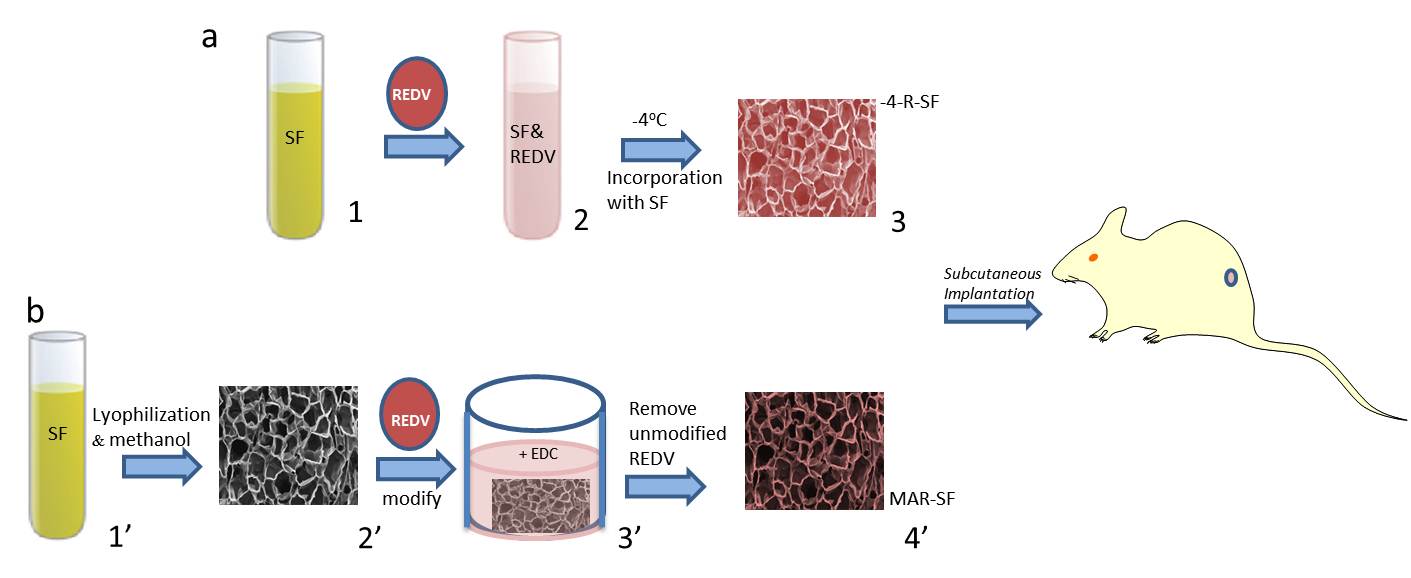
实验流程示意图:a,通过温度控制法制备丝素蛋白多孔支架的流程;b,通过EDC交联法制备丝素蛋白多孔支架的流程

